
华熙生物晚间公告,公司于2025年3月24日至2025年3月28日接受了美国食品药品监督管理局(FDA)的cGMP现场检查,涵盖质量体系、设施与设备、物料系统、生产系统、实验室系统、包装与标签六大系统,检查产品范围为玻璃酸钠原料药。近日,公司收到FDA出具的检查报告,以零缺陷(“0-483”)通过本次现场检查。此次是公司继2012年首次参与美国FDA现场检查以来,第五次通过FDA现场检查,表明公司高质量生产制造规范持续获得国际权威机构的认可。本次“零缺陷通过”为FDA对药品生产质量体系合规性的最高认可,标志着公司质量管理体系达到国际高标准。
举报 相关阅读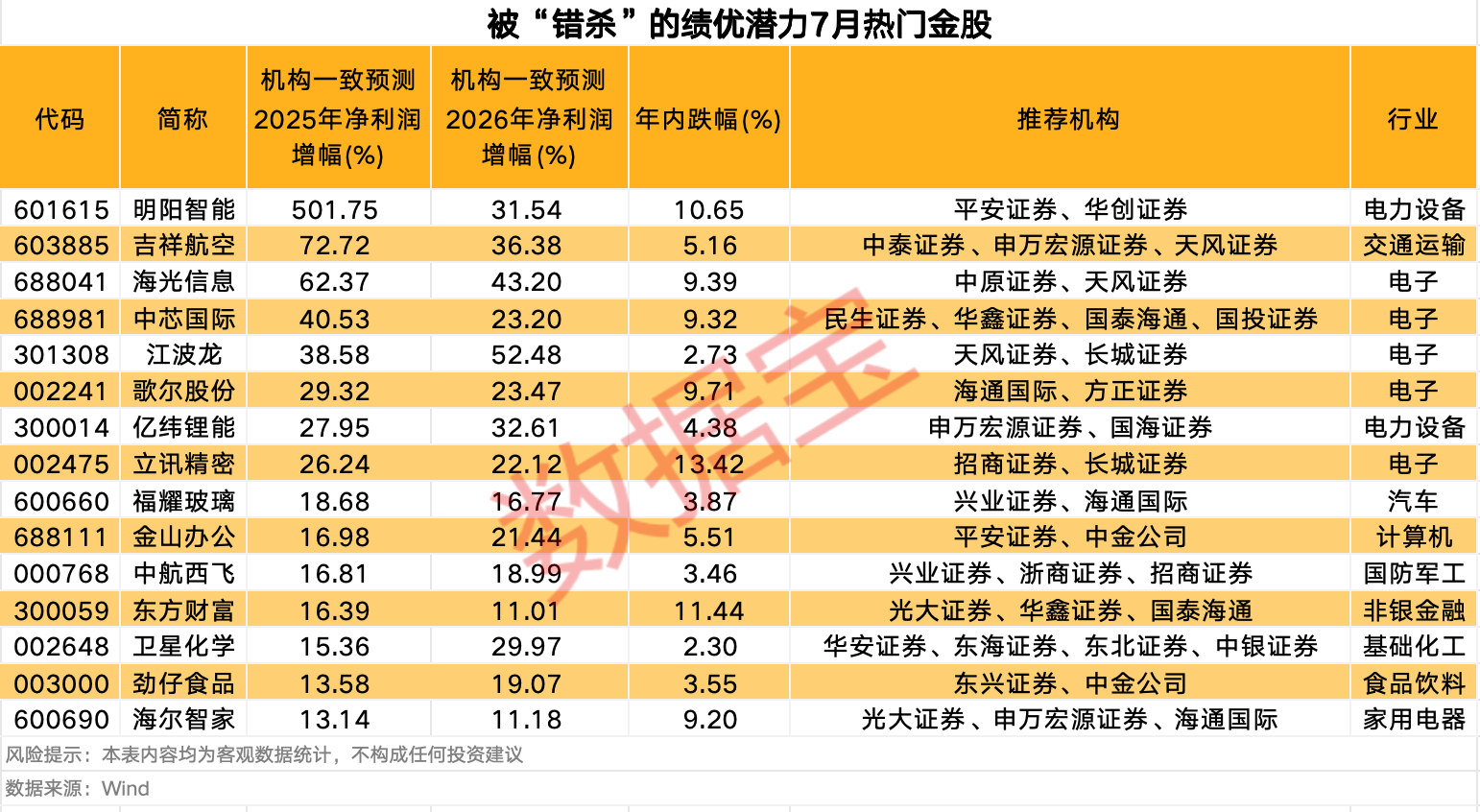 3股获机构积极关注!热门金股出炉,这些绩优潜力股或被“错杀”
3股获机构积极关注!热门金股出炉,这些绩优潜力股或被“错杀”3股获机构积极关注!热门金股出炉,这些绩优潜力股或被“错杀”
18 07-05 23:56 中证协发布2025年第二批首发企业现场检查抽查名单
中证协发布2025年第二批首发企业现场检查抽查名单中证协发布2025年第二批首发企业现场检查抽查名单
0 07-03 19:40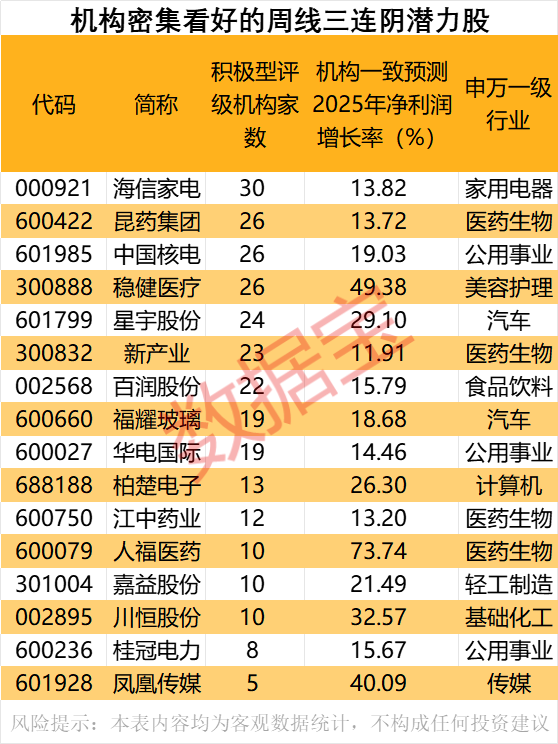 机构密集看好的周线三连阴潜力股
机构密集看好的周线三连阴潜力股机构密集看好的周线三连阴潜力股
0 06-28 12:25 猿辅导回应网传武汉员工猝死事件
猿辅导回应网传武汉员工猝死事件猿辅导回应网传武汉员工猝死事件
83 04-25 11:08 受特朗普关税政策冲击,全球市场巨震,多家公司回应相关影响
受特朗普关税政策冲击,全球市场巨震,多家公司回应相关影响在沪深交易所投资者互动平台上,多家上市公司回应“关税政策”相关影响。
153 04-07 15:59 一财最热 点击关闭易倍策略提示:文章来自网络,不代表本站观点。